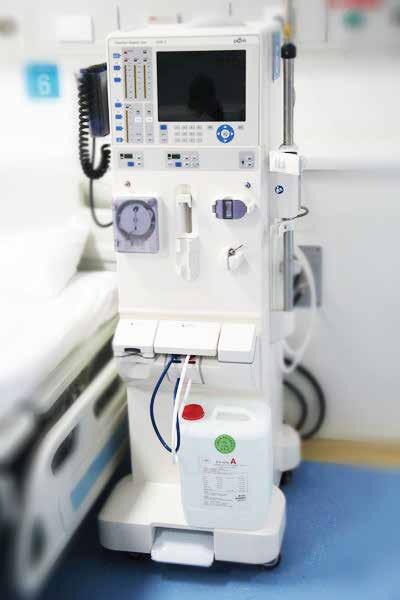
检测资质CMA、CNAS
项目类别第三方检测
服务内容生物学检测
实验室重点检测实验室
合作方式样品检测 出具报告
检测价格详细费用咨询客服
报告类型电子、纸质
检测范围全国
生物学评价方法,医疗器械的毒理学风险评估主要遵循ISO 10993-17。现行版本中描述了医疗器械可沥滤物的人体允许**的确定方法,其新修订草案中从整体框架上对产品中化学成分的毒理学风险评估进行了阐述,主要包括四个部分:危害识别、剂量-反应评估、暴露量评估、以及风险判定。即:识别器械中可能存在危害的物质,通过比较这些物质在人体中的无不良反应剂量与相应的人体暴露量,结合产品的使用情形、暴露风险、范围等,综合评估在使用过程中产品的可沥滤物对目标人群是否具有性风险。
生物学评价流程:考虑器械潜在的生物学风险,并不意味着要针对所有风险点都开展生物学测试,还可通过“评价”的方式开展物理/化学表征及毒理学风险评估、基于已有的应用历史和人体接触数据对器械的生物学风险进行评估。在近年来更新的ISO 10993-1:2018和FDA年发布的关于ISO 10993-1的应用指南中,均强调了通过化学表征测试和毒理学风险评估(ISO 10993-18和ISO 10993-17)进行生物学评价的思路,不仅可以豁免不必要的生物相容性测试及避免人力、物力和动物资源的浪费,还可以基于已有的研究数据更加充分地评估器械(尤其是持久性植入的高风险类器械)中潜在的生物性风险,从而优化生物学测试方案,达到器械性评价的目的。
生物学评价的基本原则
ISO 10993-1:2018标准的第4条款中规定了生物学评价的基本原则:
评估应包括优势/劣势的考量,并且相关于:
a) 医疗器械的配置(例如尺寸,几何形状,表面特性),并列出医疗器械的结构材料(定性),并在必要时列出医疗器械中每种材料的比例和数量(质量)(定量);
b) 各种材料的物理和化学特性及其组成;
c) 任何使用或人类接触数据的历史记录;
d) 产品和成分材料,分解产物和代谢产物的任何现有毒理学和其他生物学性数据;
e) 测试步骤
生物学评价中免于动物试验的基本条件:
1、完整充分的关于材料表征等同性及材料毒理学同性的验证资料;
2、证明医疗器械使用材料具有可论证(使用)的使用史的文献资料;
3、新产品与已上市产品人体接触形式(应用)、制造和完全相同的证明。如有不同,应有此差异不会影响生物性的分析资料和/或试验数据
生物学评价指导原则,普通可吸收缝线与带倒刺可吸收缝线的产品设计、闭合伤口的机理、性能指标等均不同,需分别开展产品性能研究、断裂强力在动物体内随时间的变化的研究、评价等,建议划分为不同的注册单元申报注册。同一企业生产的上述两类缝线若原材料、生产工艺均相同,可选择其中一种缝线开展生物相容性评价。
进行材料的生物相容性评价是测定和人体接触的、构成医疗器械的材料会引起的潜在毒性。如构成医疗器械的材料会直接或通过释放一些物质引起局部或全身生物学反应,或产生生殖和发育毒性反应等。因此,对任何用于人体的医疗器械都需要进行试验,以确保将潜在风险降至可接受的程度。
http://bjzkgxyjs.b2b168.com