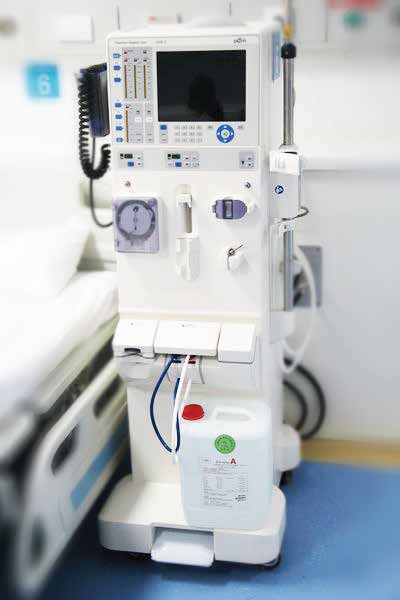
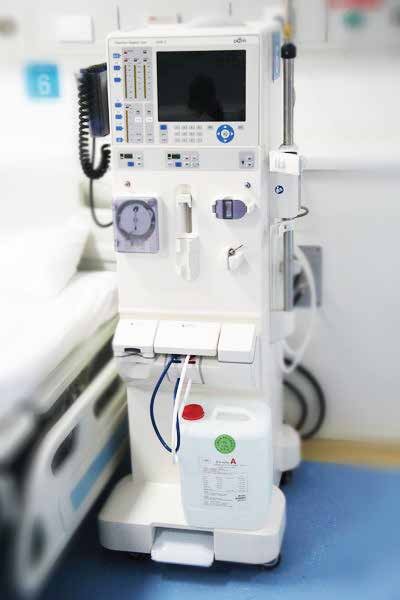
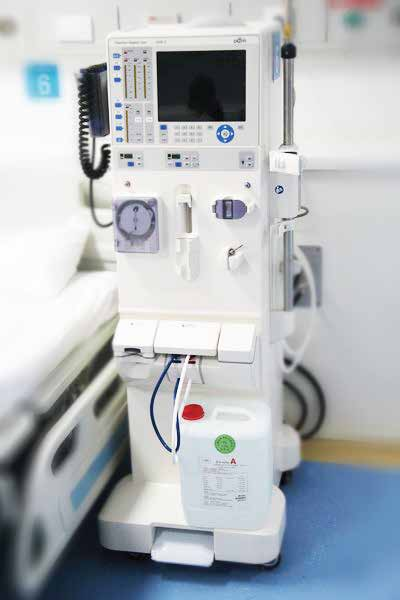
检测资质CMA、CNAS
项目类别第三方检测
服务内容生物学检测
实验室重点检测实验室
合作方式样品检测 出具报告
检测价格详细费用咨询客服
报告类型电子、纸质
检测范围全国
医疗器械生物学评价标准,医疗器械市场迅速发展,越来越多的医疗器械产品被开发并广泛应用于。医疗器械在改善患者健康方面发挥着重要作用,但也存在潜在的不良风险,必须严格。目前医疗器械生物学评价参考GB/T 16886和ISO 10993标准,从风险管理的角度阐明了医疗器械的生物学评价基本准则,要求医疗器械制造商必须遵循和质量标准,通过规范仿真测试方法,模拟并评估材料对生物组织产生的影响和作用,确保患者的。如此可见,生物学评价生物相容性测试至关重要。
通常病人监护仪的心电、体温、血氧、无创血压、有创血压、呼吸、脑电、麻醉等功能模块均含有若干个和人体接触的附件,申报附件数量较多。为便于资料的审查,建议参照如下要求:
1、参照申请表结构组成顺序,按功能模块分类,列表说明和人体接触附件的名称、接触的部位、接触时间、接触性质、生物学评价方式(豁免、评价、试验)和对应的评价资料名称、编号。
2、进行生物学试验的还应说明生物学测试项目、测试依据、测试结果、测试报告编号等内容。
3、选取有代表性附件进行测试的,应说明典型型号选取的理由。
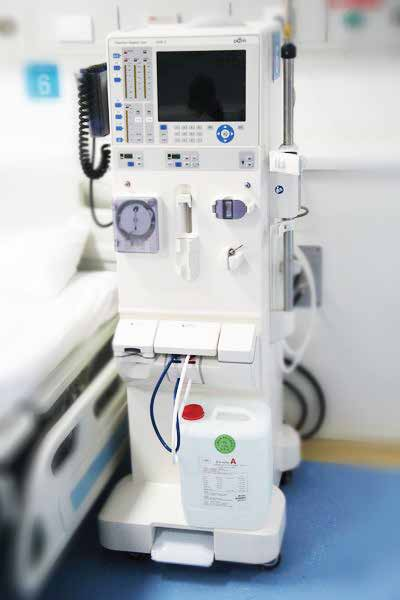
受试品与申报产品在以上所列可能影响生物相容性风险的因素中存在不一致的情况,则需提供充分的理由和证据支持所提交的试验报告适用于申报产品,必要时补充相应的生物学评价资料,如可沥滤物分析及毒理学风险评定资料、相关生物学试验项目的补充试验等。
生物学评价指导原则,普通可吸收缝线与带倒刺可吸收缝线的产品设计、闭合伤口的机理、性能指标等均不同,需分别开展产品性能研究、断裂强力在动物体内随时间的变化的研究、评价等,建议划分为不同的注册单元申报注册。同一企业生产的上述两类缝线若原材料、生产工艺均相同,可选择其中一种缝线开展生物相容性评价。
生物学评价报告通常包括以下几个方面的内容:
1)医疗器械生物学评价的策略和程序内容;
2)在风险管理计划范畴内确定材料可接受标准及预期用途;
3)充分的材料表征;
4)开展/豁免测试的说明;
5)已有数据和试验结果的解释;
6)完成生物学评价所需的补充数据;
7)器械总体生物学性的结论
生物学评价产品根据与身体接触的持续时间可分为:
1. 暂时接触器械,接触时间小于24h;
2. 短期接触器械,接触时间大于24h,小于30天;长期接触器械,接触时间大于30天。
http://bjzkgxyjs.b2b168.com