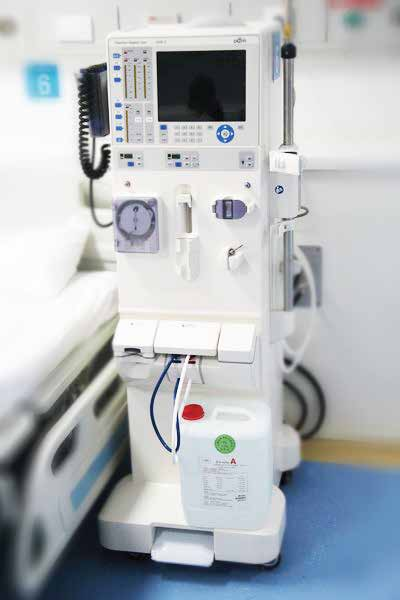
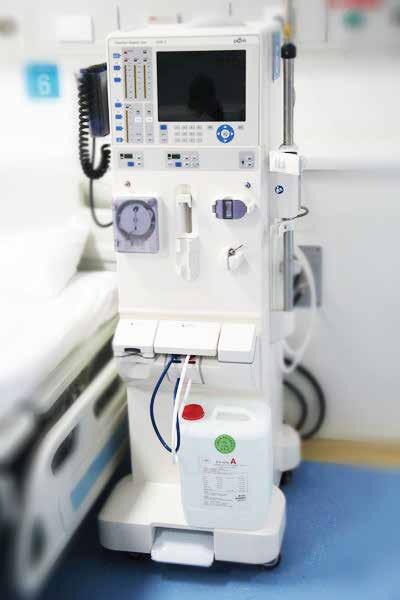
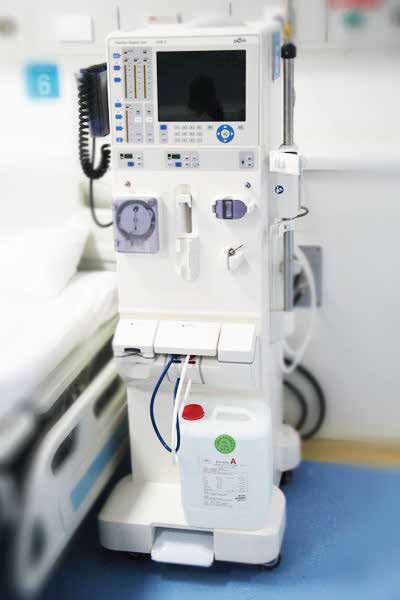
检测资质CMA、CNAS
项目类别第三方检测
服务内容生物学检测
实验室重点检测实验室
合作方式样品检测 出具报告
检测价格详细费用咨询客服
报告类型电子、纸质
检测范围全国
医疗器械生物学评价标准,医疗器械市场迅速发展,越来越多的医疗器械产品被开发并广泛应用于。医疗器械在改善患者健康方面发挥着重要作用,但也存在潜在的不良风险,必须严格。目前医疗器械生物学评价参考GB/T 16886和ISO 10993标准,从风险管理的角度阐明了医疗器械的生物学评价基本准则,要求医疗器械制造商必须遵循和质量标准,通过规范仿真测试方法,模拟并评估材料对生物组织产生的影响和作用,确保患者的。如此可见,生物学评价生物相容性测试至关重要。
需考虑重新进行生物学评价的情形:
1、制造产品所用材料来源或技术规范改变时;
2、产品配方、工艺、初包装或改变时;
3、涉及贮存的制造商使用说明书或要求的任何改变,如贮存期和运输改变;
4、产品预期用途改变时;
5、有证据表明产品用于人体后表现了不良反应时。
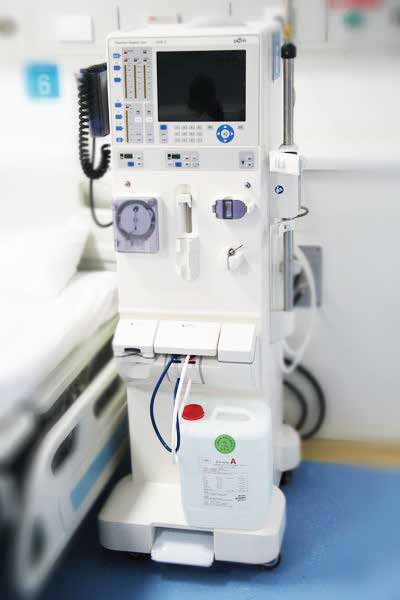
为确保使用的生物学检测性,在完成物理和化学性能、加工性能和性能等有效性要求后,必须对材料进行生物学评价试验。生物学评价建立在试验基础上,并结合医疗器械风险管理过程进行评价和试验。
生物等效性评价,可浸提物和可沥滤物研究相关的内容,例如标准中强调了分析阈值的重要性, 要确保分析方法的定量限或检出限满足分析阈值的要求。因为不同产品的接触时间和类型不同,且表面积的差异,导致分析阈值的限度差异很大且限度很低,开发合适的分析方法以满足**的要求成为化学表征领域的一大难点。
生物学评价标准分别是:GB/T16886医疗器械生物学评价,第1部分:评价与试验;第2部分:动物保护要求;第3部分:遗传毒性、致癌性和生殖毒性试验;第4部分:与血液相互作用试验选择;第5部分:体外细胞毒性试验;第6部分:植入后局部反应试验;第7部分:环氧乙烷残留量;第8部分:生物学试验参照样品的选择和定性指南;第9部分:潜在降解产物定性与定量框架;第10部分:与致敏试验;第11部分:全身毒性试验;第12部分:样品制备与参照样品;第13部分:聚合物医疗器械的降解产物定性与定量;第14部分:陶瓷降解产物定性与定量;第15部分:金属与合金降解产物定性与定量;第16部分:降解产物和可溶出物的毒代动力学研究设计;第17部分:可沥滤物允许**的确立;第18部分:材料化学表征;第19部分:材料物理化学、形态学和表面特性表征;第20部分:医疗器械*毒理学试验原则与方法;ISO/CD10993-21生物医学材料生物学评价标准编写指南。
生物学检验鉴于医疗器械或材料在器械预期用途、目标人群和人体接触等方面的特性,这些试验可能不足以证明医疗器械的性,因此有必要针对的目标,对某些医疗器械进行附加试验,如毒性试验和*毒性试验。对直接与脑组织和脑脊液接触的科医疗器械,需进行动物植入试验,以评价其对脑组织、易感性、脉络丛和蛛网膜颗粒分泌及吸收脑脊液的影响。
http://bjzkgxyjs.b2b168.com